Quant'è precisa la datazione del 14C?
Il carbonio, quella sostanza nera presente nel legno carbonizzato, esiste sotto varie forme. Una forma poco comune è chiamata «carbonio quattordici» o «radiocarbonio», o più brevemente 14C, per differenziarlo dal più comune «carbonio dodici», o semplicemente, «carbonio» (che viene scritto 12C, ed è più leggero del 14C). Molte persone sono preoccupate che il 14C provi l'inesattezza della scala biblica del tempo. Tuttavia, l'orologio del 14C è in pieno accordo con l'immagine biblica del passato della terra.
Il comune 12C è presente normalmente in natura e lo troviamo nell'anidride carbonica (che è composta da un atomo di 12C e da due atomi di ossigeno, e si indica con la sigla 12CO2 oppure semplicemente CO2) presente nell'aria che respiriamo e viene «assorbita» e assimilata dalle piante e quindi dagli animali (perché si nutrono delle piante) e da tutti gli esseri viventi, così che il nostro corpo, o la foglia di un albero, o perfino un mobile in legno, contiene carbonio.
Il 14C, invece, si forma negli strati più alti dell'atmosfera sotto l'azione dei raggi cosmici, che trasformano l'azoto in 14C; una volta formato, il 14C si comporta proprio come se fosse 12C, e lo troviamo così nell'anidride carbonica (14CO2), e di conseguenza in ogni essere vegetale e animale.
Ma la differenza tra il 12C e il 14C sta in questo: una volta formato, il 14C inizia a decadere radioattivamente, cioè a trasformarsi nuovamente in azoto, secondo dei tempi di decadimento (cioè di trasformazione) che possono essere calcolati. Se prendiamo una certa quantità d'aria, e misuriamo quanti atomi di 12C ci sono per ogni atomo di 14C, stiamo calcolando il rapporto 14C/12C. Adesso consideriamo un cucchiaino di cacao (colore marrone scuro) mescolato in un impasto di torta (colore giallo): dopo un po' che mescoliamo, il rapporto tra la quantità di cacao e le particelle di farina è approssimativamente lo stesso in ogni parte dell'impasto, così che vedremo tutto l'impasto di colore marrone chiaro (che è una via di mezzo tra i due colori iniziali), indifferentemente dalla parte di impasto esaminato. Allo stesso modo, poiché il 14C (rappresentato dal cacao) è così ben mescolato col 12C (rappresentato dalla farina) in ogni parte della natura vivente, troveremo che questo rapporto è lo stesso sia se esaminiamo una foglia d'albero (che è una parte della natura vivente) sia una parte del nostro corpo (che è un'altra parte della natura vivente).
Come funziona "l'orologio del 14C"
Appena una pianta o un animale muore, gli atomi di 14C di cui è costituito non vengono più rimpiazzati da altri nuovi come avveniva, invece, quando viveva; così la sua quantità di 14C diventa sempre più piccola col passare del tempo, perché a poco a poco il 14C decade trasformandosi in azoto. Così più passa il tempo più il rapporto 14C/12C diventa piccolo; in altre parole, c'è un orologio che inizia a ticchettare dal momento in cui qualcosa muore. Ovviamente, questo «orologio» riguarda solo ciò che una volta conteneva carbonio: per esempio, non può essere usato per datare rocce e minerali. Dalla fisica sappiamo quanto tempo impiega il 14C a decadere (cioè a trasformarsi), e così diventa possibile misurare il tempo che è passato da quando la pianta o l'animale è morto; infatti sappiamo che se abbiamo una qualsiasi quantità di 14C, in 5730 anni decadrà metà di questa quantità. Per esempio, supponiamo che al momento della morte un qualunque essere vivente aveva 20 grammi di 14C e 1000 grammi di 12C (con un rapporto 14C/12C di 20/1000; e tale rapporto era uguale per ogni altro essere vivente di quel tempo); se al giorno d'oggi, essendo passati tanti anni da quando morì, gli sono restati solo 10 grammi di 14C (perché il resto si è trasformato in azoto) rispetto ai 1000 grammi di 12C, ciò significa che il rapporto 14C/12C è diventato la metà (10/1000): sono quindi passati 5730 anni da quando morì. Tra altri 5730 anni l'individuo avrà un rapporto 14C/12C uguale a 5/1000, che equivale alla metà di quello di oggi (10/1000), e quindi un quarto di quello al momento della morte (20/1000) avvenuta 5730 anni fa. Tutto questo si può riassumere in una formula matematica:
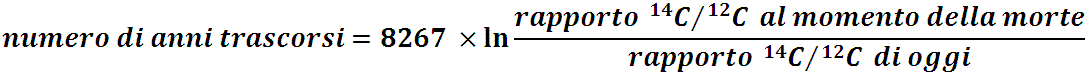
Ma come facciamo a sapere quale rapporto 14C/12C c'era al momento della morte dell'individuo? Ovviamente dobbiamo sapere questo per poter constatare in quale istante l'orologio iniziò a ticchettare. Abbiamo visto che questo rapporto sarebbe stato lo stesso di quello presente in tutta la natura vivente (come il nostro cacao che è omogeneo in ogni parte dell'impasto di torta) di quel periodo; ma come facciamo a sapere quanto era? Gli scienziati suppongono che il rapporto 14C/12C nell'atmosfera di ieri fosse lo stesso di quello che c'è oggi? Non esattamente. È un fatto accertato che la rivoluzione industriale, con la sua combustione di ingenti masse di carbone, abbia turbato il naturale bilancio del carbonio, per esempio rilasciando ingenti quantità di 12C nell'aria. Studi sugli anelli degli alberi possono dirci qual era il rapporto 14C/12C prima della rivoluzione industriale, e tutta la datazione del 14C viene fatta tenendo conto di questo. Ma si suppone che prima della rivoluzione industriale il rapporto sia stato costante e uniforme per molto tempo. Ma è corretta questa supposizione (poiché da esso dipende la validità del sistema)? Perché W.F.Libby, il brillante scopritore di questo metodo, suppose ciò? Sappiamo che il 14C entra continuamente nell'atmosfera (e dunque negli esseri viventi) perché l'azoto viene trasformato in 14C, e sappiamo anche che il 14C lascia continuamente l'ambiente perché, essendo radioattivo, si ritrasforma in azoto. Consideriamo la seguente tabella:
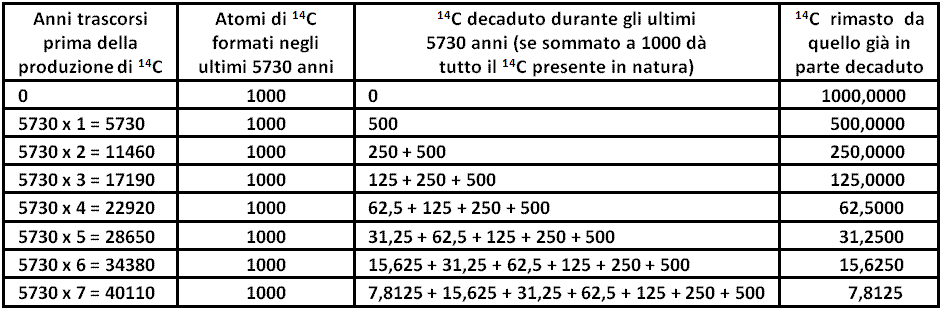
In questa tabella immaginiamo che si ogni 5730 anni si formino, in modo costante e uniforme, 1000 (per semplificare) nuovi atomi di 14C (5730 anni sono il periodo entro cui metà della quantità di 14C «scompare» perché si trasforma in azoto).
Nell'anno 0 (cioè nell'anno in cui sotto l'azione dei raggi cosmici si sono formati i primi 1000 atomi di 14C), poiché non sono ancora passati 5730 anni non decade alcun atomo.
Trascorsi 5730 anni, decadono 500 atomi di 14C (che facevano parte dei primi 1000), per cui
• la differenza tra gli atomi di 14C formati negli ultimi 5730 anni e gli atomi di 14C decaduti nello stesso periodo è 1000 – 500 = 500;
• di quelli formatisi nell'anno 0 ne restano 500, i quali, sommati a quelli che si stanno formando nel periodo considerato (cioè altri 1000 atomi), danno un totale di 500 + 1000 = 1500 atomi di 14C presente nell'ambiente.
Nell'anno 11460 (dunque, trascorsi altri 5730 anni), decade, invece, la metà (500) del 14C formatosi nell'anno 5730 (in cui si erano formati altri 1000 atomi), ma poiché abbiamo detto che nell'anno 5730 sono rimasti 500 atomi del 14C formatosi nell'anno 0, di questi 500 ne decadranno la metà (250), per cui sono scomparsi 500 + 250 = 750 atomi di 14C; per cui
• la differenza tra gli atomi di 14C formato negli ultimi 5730 anni e gli atomi di 14C decaduto negli ultimi 5730 anni è 1000 – 750 = 250;
• di quelli formatisi nell'anno 0 ne restano 250; di quelli formatisi nell'anno 5730 ne restano 500; quelli formatisi nell'anno considerato sono 1000; quindi 250 + 500 + 1000 = 1750 atomi di 14C presenti nell'ambiente.
Nell'anno 17190 (dunque trascorsi ancora 5730 anni), decade, invece, la metà (500) del 14C formatosi nell'anno 11460 (in cui si erano formati altri 1000 atomi), ma poiché nell'anno 11460 sono rimasti 500 atomi del 14C formatosi nell'anno 5730, di questi 500 ne decadranno la metà (250); inoltre, come abbiamo detto, nell'anno 11460 sono rimasti 250 atomi del 14C formatosi nell'anno 0, di questi 250 ne decadranno adesso la metà (125), per cui sono scomparsi 500 + 250 + 125 = 875 atomi di 14C; dunque
• la differenza è 1000–875=125;
• di quelli formatisi nell'anno 0 ne restano 125; di quelli formatisi nell'anno 5730 ne restano 250; di quelli formatisi nell'anno 11460 ne restano 500; quelli formatisi nell'anno considerato sono 1000; quindi 125+250+500+1000=1875 atomi di 14C presenti nell'ambiente.
Lo stesso ragionamento va seguito per tutti gli altri anni che seguono. Va notato che più avanti si va negli anni più si appiattisce la nostra differenza, raggiungendo valori sempre più piccoli che possono essere approssimati a zero: ciò significa che andando avanti nel tempo decade tanto 14C prodotto in un periodo quanto se ne produce nello stesso periodo, per cui si raggiungerà un costante stato stazionario in cui ogni 5730 anni si produrranno 1000 atomi di 14C e ne decadranno altri 1000 con una differenza dello 0%; e saranno presenti nell'ambiente sempre 2000 atomi di 14C, cioè i 1000 formati nell'ultimo periodo più tutte le frazioni rimaste degli altri periodi già trascorsi.
Libby, in accordo con la maggior parte degli scienziati a lui contemporanei, suppose che questo stato stazionario fosse stato raggiunto molto tempo fa, e che il 14C starebbe adesso entrando e uscendo dal sistema nelle stesse quantità. Perché? Perché i calcoli mostrano che ci vorrebbero solo 30.000 anni (dalla prima volta che i raggi cosmici iniziarono a bombardare l'atmosfera) affinché con buona approssimazione si inizi a vedere uno stato stazionario, ma già molto tempo prima di Libby i geologi ed altri avevano convinto la maggior parte della gente che la terra fosse molto, molto più vecchia di 30.000 anni. In altre parole, il 14C avrebbe dovuto già raggiungere lo stato stazionario già da molti milioni di anni, per poter confermare un'età della terra così vecchia.
Cosa mostrano le misure?
Aveva ragione Libby? Ai suoi tempi, le misure di cui egli era informato mostravano che il 14C stesse entrando nel sistema circa il 12% più velocemente di quanto non stesse uscendo. Ciò voleva indicare che il sistema aveva meno di 30.000 anni, perché lo stato stazionario non era stato ancora raggiunto (infatti non era lo 0% ma il 12%). Ma tale discrepanza rientrava nelle stime dell'errore sperimentale fatte da Libby, e così poteva essere ignorata. Alcuni hanno addirittura suggerito l'idea che Libby abbia premeditatamente considerato un margine di errore così grande, in modo da poter racchiudere il risultato attuale.
Che c'è da dire riguardo alle misure moderne e più sofisticate? Sfortunatamente per i difensori della terra vecchia, queste misure continuano a sostenere una netta differenza fra la quantità che si produce e quella che decade. Per esempio, le seguenti cifre date dai chimici nucleari Fairhall e Young suggeriscono che ci sia addirittura una differenza di circa il 50% (e non del 12%).
«Notiamo incidentalmente che l'inventario naturale totale del 14C... corrisponde a un tasso di decadimento di 14C di 1,63 x 104 atomi / (metro2 x secondo) sulla terra, notevolmente al di sotto della media del tasso di produzione di atomi di 14C calcolata sugli ultimi 10 cicli solari (111 anni) di 2,5 x 104 (+ 0,5 x 104) atomi / (metro2 x secondo)... La fonte della discrepanza è... sconosciuta a meno che il tasso di produzione odierno sia proprio significativamente più alto del tasso di produzione media...» (Fairhall, A.W. e Young, J.A., 1970. «Radionuclides in the Environment», Advances in Chemistry, vol. 93, p. 402).
Tuttavia, ci sono molte complessità e imprecisioni in queste misure. Alcuni hanno adottato un nuovo modello non uniforme basato su una differenza media di circa il 35%, per stabilire una scala di ricalibrazione che vorrebbe far intendere che le date più vecchie devono essere ridotte più grandemente delle più recenti. Questo sembra buono a primo sguardo, poiché stabilirebbe un limite all'età dell'atmosfera terrestre di circa 7.000-10.000 anni. Tuttavia, si deve procedere con grande cautela perché il modello potrebbe essere troppo semplicistico. Per esempio, come facciamo a sapere che il «mescolamento del pasticcio di torta» era realmente completo? Il carbonio presente alla superficie dell'oceano è in bilancio con quello in profondità? Quali sono i possibili errori nelle stime dei tassi di influsso/efflusso di 14C? E così via. Dati storici e dati degli anelli degli alberi suggeriscono che i risultati totali sono più complessi di quanto si possa pensare a colpo d'occhio.
È importante considerare tre altri possibili effetti:
- 1. Se, come la maggior parte dei creazionisti propone, ci fu un enorme distesa di vapore acqueo attorno alla terra prima del Diluvio, questa avrebbe protetto l'atmosfera da certe radiazioni cosmiche. Perciò, la quantità di 14C nel mondo pre-diluviano sarebbe stata molto minore di quella odierna. Così, un campione prediluviano potrebbe apparire molto vecchio, o perfino di età infinita, perché aveva così poco 14C in esso, facendolo sembrare come se fosse decaduto da decine di milioni di anni. La maggior parte del carbone è vegetazione che crebbe prima del Diluvio e fu seppellita dal Diluvio, perciò non deve sorprendere il fatto che il carbone e l'olio pre-diluviani non avrebbero virtualmente 14C da essere misurato.
- 2. Il decadimento esponenziale del campo magnetico della terra come descritto dal Dr. Thomas Barnes ci suggerisce che andando indietro nella storia, la forza del campo cresce rapidamente. Un campo magnetico più forte significherebbe più protezione contro i raggi cosmici, perciò, molto meno 14C prodotto e, di conseguenza, questo darebbe vecchie età quanto più si va indietro nel tempo.
- 3. Alcune ricerche recenti, sebbene controverse, hanno sollevato l'interessante suggerimento che la velocità della luce sia diminuita nei tempi della storia. Se ciò è corretto, allora il tasso di decadimento radioattivo sarebbe automaticamente influenzato e mostrerebbe età più alte.
Riassumendo dunque:
- 1. Il 14C sulla terra non è in uno stato stazionario, ma si sta ancora accumulando. Ciò non è in accordo con un'atmosfera molto vecchia.
- 2. Sulla base dell'evidenza disponibile al momento, le più vecchie date del 14C del modello uniforme (uniforme nel senso che ignora ogni possibile variazione del campo magnetico, della velocità della luce, ecc.) scorretto ancora oggi in uso andrebbero corrette, nel qual caso ci sarebbe un restringimento in queste date. Più vecchia è la data, maggiore è la riduzione.
- 3. La distesa protettiva di vapore acqueo e il maggiore campo magnetico prima del Diluvio potrebbero farci intendere che i livelli del 14C erano molto più piccoli che al presente, causando così risultati erronei.
- 4. Anche qualche cambiamento nelle costanti atomiche, come una luce più veloce nel passato, ridurrebbe effettivamente le età radioattive.
Imbarazzi dalle date giovani:
In ogni caso, perfino lo scorretto modello uniforme ha dato, in molti casi, seri imbarazzi all'evoluzionista dando età molto più giovani di quelle che egli si aspetterebbe seguendo il suo modello di storia della terra. Consideriamo questo: se un campione è vecchio più di 50.000 anni, è stato calcolato che avrebbe una così piccola quantità di 14C che per motivi pratici mostrerebbe un'età infinita di radiocarbonio. Così ci si aspettava che la maggior parte dei depositi come carbone, gas, ecc. fosse indatabile attraverso questo metodo. Ma nei fatti, delle migliaia di dati nei giornali Radiocarbon e Science nel 1968, solo una manciata è stata classificata «indatabile»: altro che la maggior parte! Questo è evidente in special modo in campioni di carbone e gas prodotti presumibilmente nel periodo Carbonifero 300 milioni di anni fa! Ecco alcuni esempi di date che contraddicono le vedute evoluzionistiche:
Il carbone della Russia del periodo «Pennsylvaniano», presumibilmente di 300 milioni di anni, è stato datato col metodo del 14C a 1680 anni. (Radiocarbon, vol. 8, 1966)
• Il gas naturale dell'Alabama e Mississippi (Cretaceo ed Eocene, rispettivamente) dovrebbe avere da 50 milioni a 135 milioni di anni, tuttavia il 14C dà dati di 30.000 a 34.000 anni rispettivamente (Radiocarbon, vol. 8, 1966)
• Le ossa di una tigre a denti a sciabola dei pozzi di catrame di LaBrea (vicino a Los Angeles) presumibilmente da 100.000 a un milione di anni, dava una data di 28.000 anni. (Radiocarbon, vol. 10, 1968).
Altri fatti del 14C:
In aggiunta ai risultati sopra citati, ci sono altre possibili fonti di errore nella datazione del 14C. Alla luce di tutto ciò, sarebbe proprio rischioso insistere che una data del 14C rappresenti la verità assoluta, specialmente se contraddice i chiari insegnamenti della Scrittura. Consideriamo questi esempi:
• Una foca ammazzata da poco tempo datata attraverso il 14C mostrava di essere morta 1300 anni fa. (Antarctic Journal, vol. 6 [Settembre-Ottobre 1971], p. 211).
• Conchiglie di mollusco vivente erano datate fino a 2.300 anni fa. (Sciences, vol.141, 1963, pp. 634-637).
• Conchiglie di lumache viventi mostravano di essere morte 27.000 anni fa. (Science, vol. 224, 1984, pp. 58-61).
Non indugiamo ad aggiungere che di solito si possono scoprire le ragioni di questi risultati anomali, per esempio, considerando l'attività del 14C in carbonati disciolti in acqua, ecc. Ma quando si esamina un campione di età sconosciuta vissuto in un ambiente che non sappiamo com'era al momento della morte del campione, come possiamo escludere tali tipi di risultati? Una citazione presa da un giornale antropologico di riguardo pone luce sulla natura del problema: «Gli intrighi del metodo di datazione del 14C sono innegabilmente profondi e seri... Non sarebbe una sorpresa, allora, che almeno metà della datazioni siano rifiutate. La meraviglia è, sicuramente, che la restante metà viene ad essere accettata». (Lee, R. E., Radiocarbon, «Ages in Error», Anthropological Journal of Canada, 1981, vol. 19, No. 3, p. 9). Dunque, vediamo che il metodo della datazione del 14C non impallidisce per niente il creazionista biblico che crede in una terra giovane. Infatti, quando questo metodo viene pienamente capito in accordo con i dati moderni, sembra appoggiare tale convinzione.
Tratto da The Answer Book, Revised Edition, di Ken Ham, Andrew Snelling e Carl Wieland, pubblicato da Master Books, 1992. Tradotto, rielaborato e semplificato dallo staff di eVangelo. Fornito da Answers in Genesis Copyright 1996, Creation Science Foundation, All Rights Reserved – eccetto come osservato sull'annessa pagina «Usage and Copyright» che accorda agli utenti di ChristianAnswers.net i generosi diritti di esporre questa pagina per operare nelle loro case, testimonianza personale, chiese e scuole.
Data: 25/05/2002
Visite: 15694 | |


|
|